中药新药步入丰收期,研发上仍存在痛点
近年来,随着国家推动中医药发展的相关政策落地,以及技术指导原则的不断完善,中药新药研发步入丰收期。
米内网数据显示,近年来中药新药获批品种数、申报上市品种数及申报临床品种数均呈逐年递增态势,尤其是2020年新版中药注册管理办法实施后,中药1类新药的申报呈现井喷的态势,至今已有超过80个品种(含原料药,下同)提交临床/上市申请,其中9个已获批生产。
图1:近年来获批生产、申报上市及申报临床的中药新药数量(含原料药)
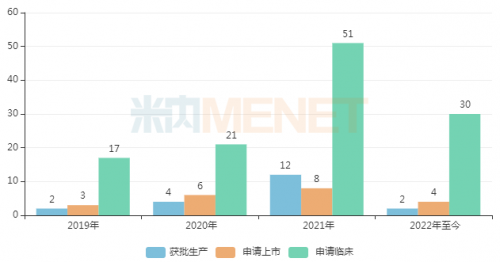
注:获批日期以审评结论日期计,数据统计截至7月27日
来源:米内网MED2.0中国药品审评数据库
与化学药、生物药相比,中药新药研发难度更大,因为其物质基础及药理机制更为复杂,对其安全性、有效性等方面的研究,需要新方法新技术。因此,虽然目前中药新药研发火热,但在研发上仍存在不少难题与痛点。
“从临床的角度看,中药新药研发存在很多机遇和挑战,包括新的注册分类需要形成新的研究模式,以患者为中心的中药研发尚需努力,中药新药研究的基础问题也需要引起重视,同时一些桎梏必须打破,包括‘组方合理性’的创新悖论、‘辨证论治’的束缚、‘毒性药材’的困境以及‘优势病种’的困惑等。”在2022米思会分会——盈科瑞独家协办的[米交汇]中药创新研发生态合作论坛上,上海中医药大学张磊教授说道。
而谈到中成药在临床应用中的困境,北京大学药学院杨秀伟教授表示:“中成药有效物质不清楚、作用机理和量效不明确、临床有效性评价不充分,如何用现代医学进行阐明,这是一个比较大的挑战。”
“中医药迎来了发展利好的全新时期,但目前中医药产业距离国务院提出的中医药高质量发展目标还存在距离,尤其是在科技竞争力,研究创新性等方面存在不足。”中国中医科学院中药研究所研究员、博士生导师、北京盈科瑞创新医药股份有限公司董事长张保献如是说。
制剂改良、中药复方。。。。。。中药新药研发可以这样做
2020年新版中药注册管理办法将中药分为4类,包括1类中药创新药、2类中药改良型新药、3类古代经典名方中药复方制剂及4类同名同方药。
“中药新制剂的开发,有别于全新药物开发的原始创新,中药制剂创新可以在已明确有临床获益的产品上进行创新,更容易获得成功。”张保献教授说道。站在巨人肩膀上开展的中药制剂改良不失为中药研发的一条捷径,例如盈科瑞采用纳米凝胶技术可以改善外用药物在靶部位的透皮效果,增加在靶部位的驻留时间,提高效果;雾化吸入制剂可直接作用于呼吸道,具有起效迅速、疗效佳、给药剂量小、全身不良反应少、适合特殊群体使用等优势。
在新冠疫情阻击战中,中医药因能有效缓解症状、减少轻症向重症发展、提高治愈率、促进恢复期人群机体康复等而备受关注,以“三药三方”为代表的一批中医药疗法被证明具有明显疗效。
“大疫出良方,‘三药三方’的成功获批,是基于临床和市场需求的中药新药研发新思路。中药复方的研究是推动中医药现代化的重要环节之一。”杨秀伟教授认为,中药新药的开发应立足于经典名方,在中医药理论指导下,采用现代技术,阐明作用机理,才能“多、快、好、省”地开花结果。
在2022米思会分会——盈科瑞独家协办的[米交汇]中药创新研发生态合作论坛上,北京盈科瑞创新医药股份有限公司总裁张宏武表示,在中药新药研发中,有两点因素很重要:一是专业的团队,二是创新体系。目前盈科瑞拥有以张保献教授为代表的一批国家顶级专家,科研项目管理为研发管线执行组长全链条、全生命周期管理制。从项目立项、实施、中试生产、注册、获批、产业化全方位协调管理,以社会公认里程碑为目标,为中医药创新赋能。
浙江维康药业股份有限公司副总裁戴德雄也提到,生产企业除了要做好生产和销售外,也要和盈科瑞这样的专业研发机构合作,加大对研发的投入,做出更多符合临床需求的新药。
中药新药研发要以患者为中心,以临床价值为导向
中药新药研发要以患者为中心,以临床价值为导向,从临床需求出发研发出来的中药新药将更具竞争力。
“中医药的创新不能在相同的适应症里内卷,而要针对未满足的临床需求来进行突破,否则会造成资金、技术和临床资源的浪费。”张保献教授强调说,应该以科学的态度和科学的方法促进中医药产业的创新,强化临床需求导向,推动中药产品研发传承创新,提高中药产业发展的活力。
“要以临床需求来带动中药新药研发创新,从适应症领域来看临床需求较为常见。”张磊教授建议,可先选定关心的领域,再选择合适的适应症,之后全面收集所有该适应症的指南、共识、高质量证据,以循证医学的方法分析找出该适应症需要解决的临床问题,最后找出中药解决这些问题的基础与预期。
创新药“出海”大势所趋,中药新药国际化之路怎么走?
3月29日,国务院办公厅印发的《“十四五”中医药发展规划》中提到,要加快中医药开放发展,逐步完善中医药“走出去”相关措施,开展中医药海外市场政策研究,助力中医药企业“走出去”,推动中药类产品海外注册和应用。
2020年以来,中医药在全球疫情防控中发挥了不可或缺的作用,此次的疫情向全球展现了中医药的特色与优势,为中医药走出国门、走向世界提供了一个很好的契机。然而,中医药要想真正实现国际化,关键还是要以中医临床优势病种为目标,研发符合国际注册标准规范的药品来破冰欧美等主流市场。
但是,中成药要到海外注册上市绝非易事,尤其是在美国市场,至今仍未实现零的突破。按照FDA的《植物药指南》,中成药可以经进一步研究成为植物药。虽然FDA先后出台不少政策支持植物药进入美国市场,但其在含多成分的植物药的审评审批仍旧非常谨慎。
“植物药成分多且复杂、有效成分无明确定义、成分容易发生变化等,在质量、安全性、有效性等标准上难以明确,这给FDA的审评审批带来很大的挑战。”美国FDA前资深临床审评官姚毅博士解释道。
虽然中药国际化前路漫漫,但已有以神威药业、以岭药业、天士力、兰州佛慈等为代表的一批中药企业主动申请国际高端认证。目前已有多款中药获得FDA批准,在美国开展不同阶段的临床研究,包括天士力的复方丹参滴丸、康缘药业的桂枝茯苓胶囊、康莱特的康莱特注射液、北大维信的血脂康胶囊等。
“FDA在对植物药的审评审批上,非常注重质量,包括生产体系、种植体系等,临床上先关注安全性再关注有效性。如果在临床开发过程中,植物药的物质或产品发生变化,可能需要进行非临床桥接研究。”姚毅博士认为,选择正确的适应症(在临床前就针对临床需求设计好)、完善的III期临床(Batch-to-batch variations的桥接试验)及良好的临床结果,可大大提高植物药获得FDA批准的几率。
“盈科瑞创新医药立足于中医药,继续延伸产业链条,完善研发体系,不断丰富研发管线,用源源不断的具有临床价值的产品承载盈科瑞的技术内涵,盈科瑞愿意与广大同行优势互补、强强联合、精诚合作、共铸辉煌。”张保献教授补充道。


 渝公网安备 50023602000380号
渝公网安备 50023602000380号